Segurança e dosagem
PERFIL DE SEGURANÇA
O TAVNEOS demonstrou um perfil de segurança aceitável2,3
As reações adversas mais comuns observadas em um estudo pivotal, fase 3 em pacientes tratados com TAVNEOS foram:

Náusea
23.5%

Cefaléia
20.5%

Diminuição na contagem de leucócitos
18.7%

Nasofaringite
15.1%

Diarreia
15.1%

Vômito
15.1%

Infecção do
trato respiratório superiortract infection
14.5%

As reações adversas graves mais comuns são alterações da função hepática (5,4%) e pneumonia (4,8%)1
No pós-comercialização: foram relatados (frequencia desconhecida) lesão hepática induzida por medicamento e síndrome do desaparecimento dos ductos biliares

TAVNEOS é um substrato da CYP3A4, mas interações clinicamente relevantes são improváveis quando o TAVNEOS é coadministrado com indutores ou inibidores dessa enzima1
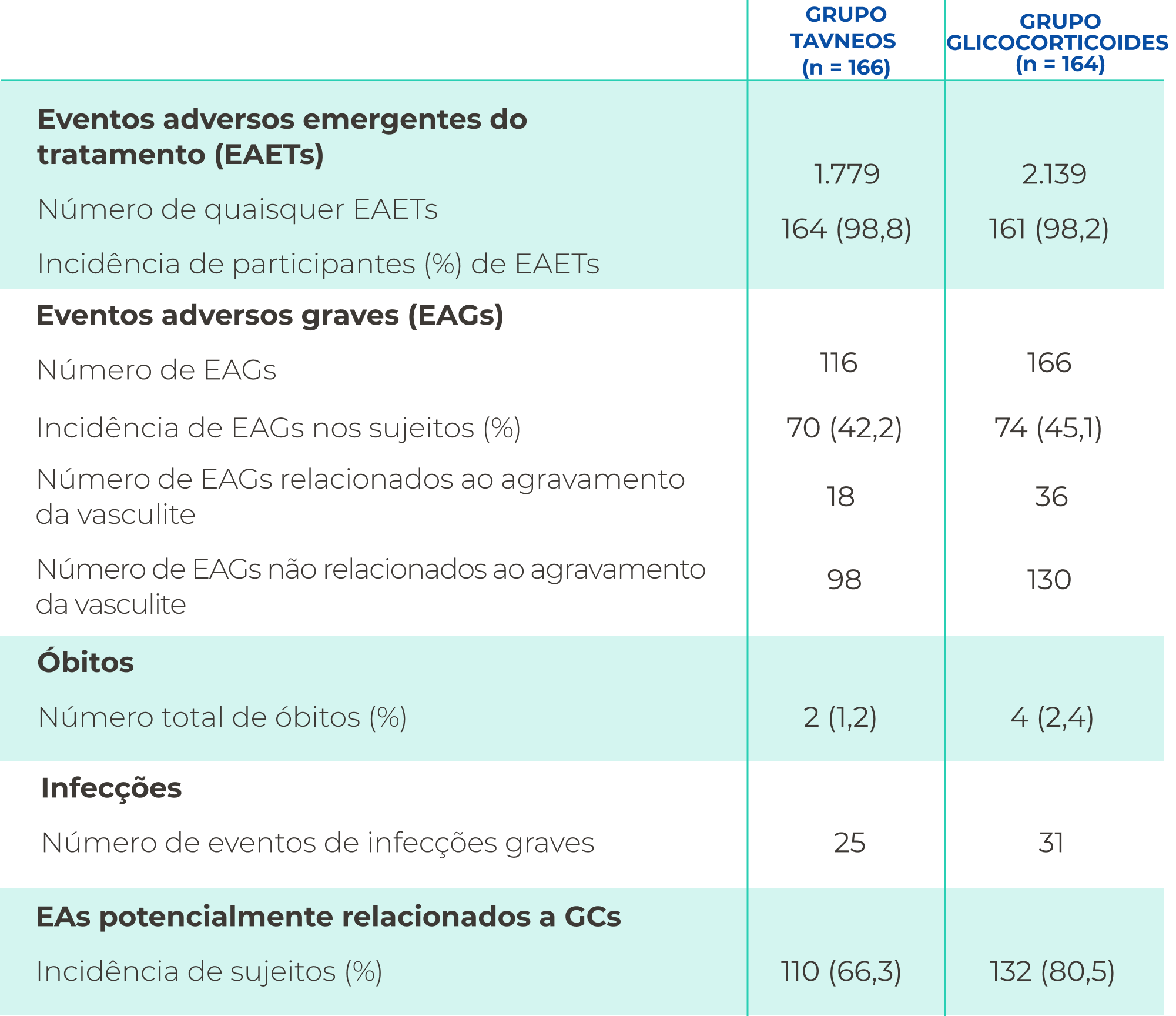
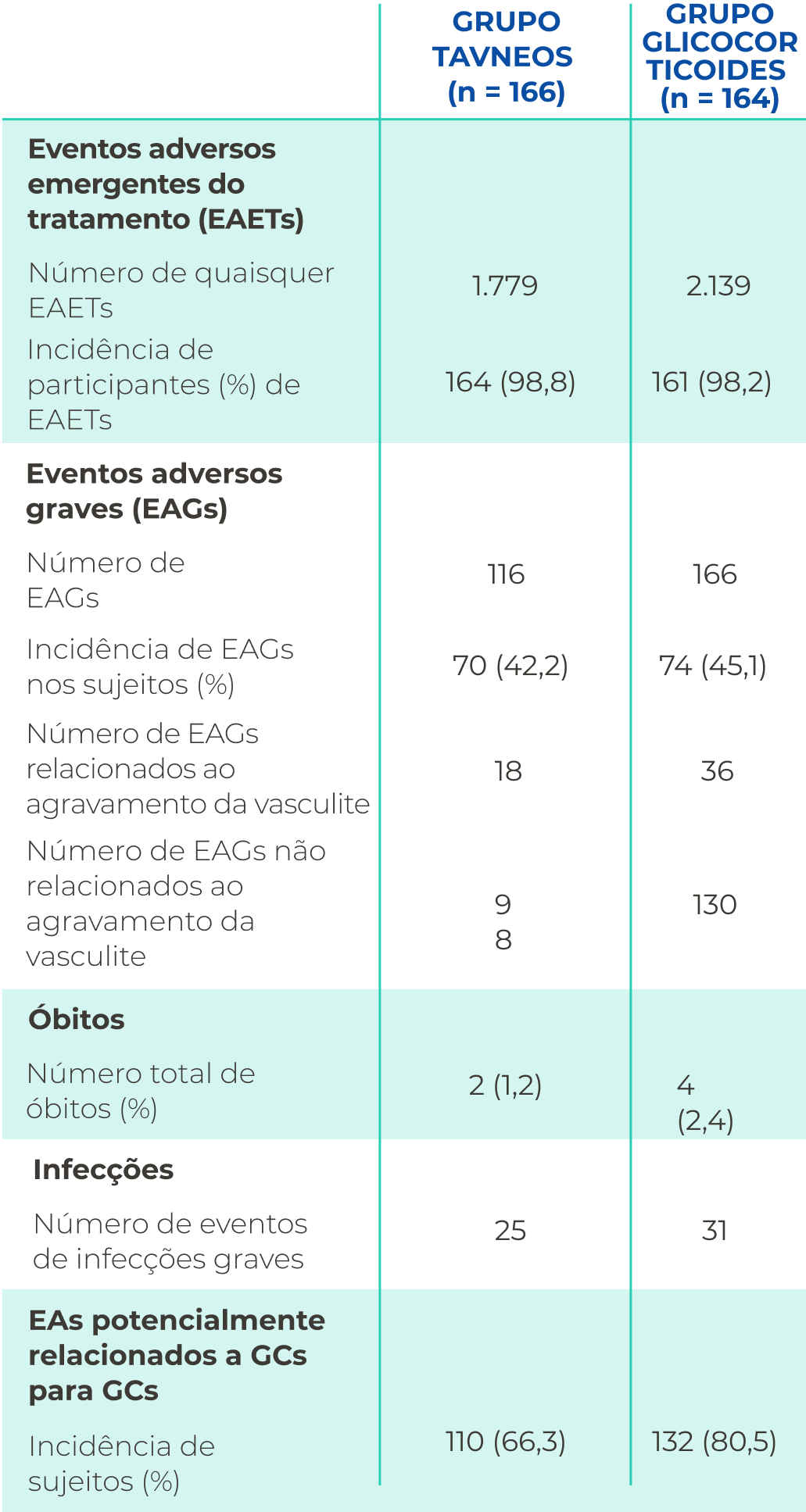
RESULTADOS DE SEGURANÇA COMPARÁVEIS

A incidencia de EAGs observada foi numericamente semelhante nos regimes à base de TAVNEOS e de GCs2

Na análise de segurança agregada, a primeira taxa de incidência de EA em pacientes, taxa de EA, taxa de EAGs, taxa de evento de infecção e taxa de redução de contagem de leucócitos foram estatisticamente menores no grupo TAVNEOS em comparação ao grupo que recebeu GCs GC4
DOSE FIXA VIA ORAL E MONITORAMENTO

TAVNEOS é tomado em dose oral fixa, com o monitoramento necessário1
TAVNEOS deve ser administrado da seguinte forma:1

30 mg TAVNEOS

duas vezes ao dia

Com alimentos
Os pacientes devem ser monitorados quanto a:
- Transaminases hepáticas e bilirrubina total pelo menos a cada quatro semanas após o início da terapia durante os primeiros 6 meses de tratamento e, posteriormente, conforme clinicamente indicado1*
- Contagem de leucócitos conforme clinicamente indicado e como parte do acompanhamento de rotina do paciente1†

Regime de tratamento em combinação com imunossupressores (RTX ou CYC/AZA)1
Referências e notas de rodapé
Notas de rodapé
*O tratamento deve ser reavaliado clinicamente e temporariamente interrompido se ALT ou AST for >3x LSN. O tratamento deve ser temporariamente suspenso se ALT ou AST for >5× LSN. Consulte a bula do produto para obter informações sobre a descontinuação permanente.1
†O tratamento deve ser temporariamente interrompido se o paciente desenvolver leucopenia (contagem de leucócitos <2×109/l), neutropenia (neutrófilos <1×109/l) ou linfopenia (linfócitos <0,2×109/l).1
Abreviações
VAA, vasculite associada ao ANCA; EA, evento adverso; ALT, alanina transaminase; ANCA, anticorpo anticitoplasma de neutrófilos; AST, aspartato transaminase; AZA, azatioprina; CYC, ciclofosfamida; CYP3A4; Citocromo P450 3A4; GC, glicocorticoide; GPA, granulomatose com poliangeíte; PAM, poliangeíte microscópica; RTX, rituximabe; EAG, evento adverso grave; EAET, evento adverso emergente do tratamento; LSN, limite superior normal; GBS,glóbulos brancos do sangue.
References
- TAVNEOS EU SmPC janeiro de 2025.
- Jayne D, et al. N Engl J Med 2021;384(7):599–609.
- European Medicines Agency (2021). An overview of Tavneos and why it is authorised in the EU. Available at: https://www.ema.europa.eu/en/documents/overview/tavneos-epar-medicine-overview_en.pdf. Data de acesso: janeiro de 2025.
- Jayne D, et al. J Am Soc Nephrol 2022:33.
▼ Este produto medicinal está sujeito a monitoramento adicional. Isso permitirá a rápida identificação de novas informações de segurança. Os profissionais de saúde são solicitados a relatar quaisquer suspeitas de reações adversas.
BR-AVA-2500003 | Data de preparação: julho de 2025