Eficácia
ALCANCE UM MELHOR CONTROLE DA DOENÇA COM UM TRATAMENTO DIRECIONADO E INOVADOR PARA GPA/PAM1–4
Desfecho primário
MELHOR CONTROLE DA DOENÇA

O regime baseado em TAVNEOS demonstrou não inferioridade na remissão clínica na semana 26 e superioridade na remissão clínica sustentada na semana 52 versus um regime baseado em GC2*
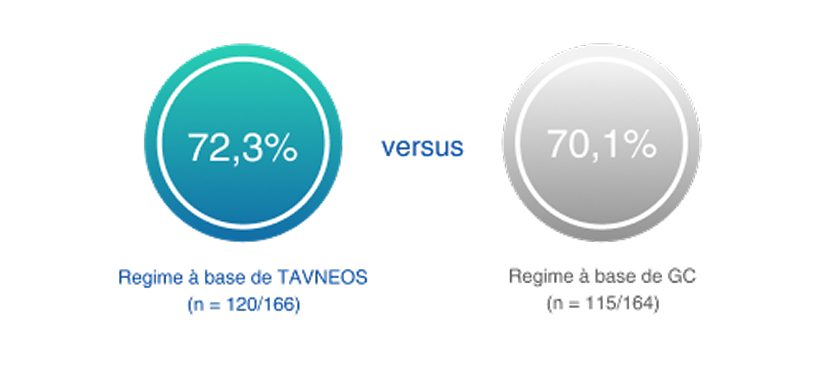
Na semana 26, o regime baseado em TAVNEOS demonstrou não inferioridade em atingir a remissão clínica versus o regime baseado em GC2
p<0,001 para não inferioridade
(Diferença 3,4, IC de 95%, -6,0 a 12,8)
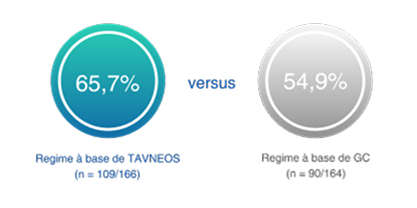
Na semana 52, o regime baseado em TAVNEOS demonstrou superioridade na remissão clínica sustentada versus um regime baseado em GC2
p=0,007 para superioridade
(Diferença 12,5, IC de 95%, 2,6 a 22,3)

Na semana 52, o regime baseado em TAVNEOS demonstrou um número necessário para tratar (NNT) entre 8 e 10†
Desfecho secundário
REDUÇÃO DO RISCO DE RECIDIVA

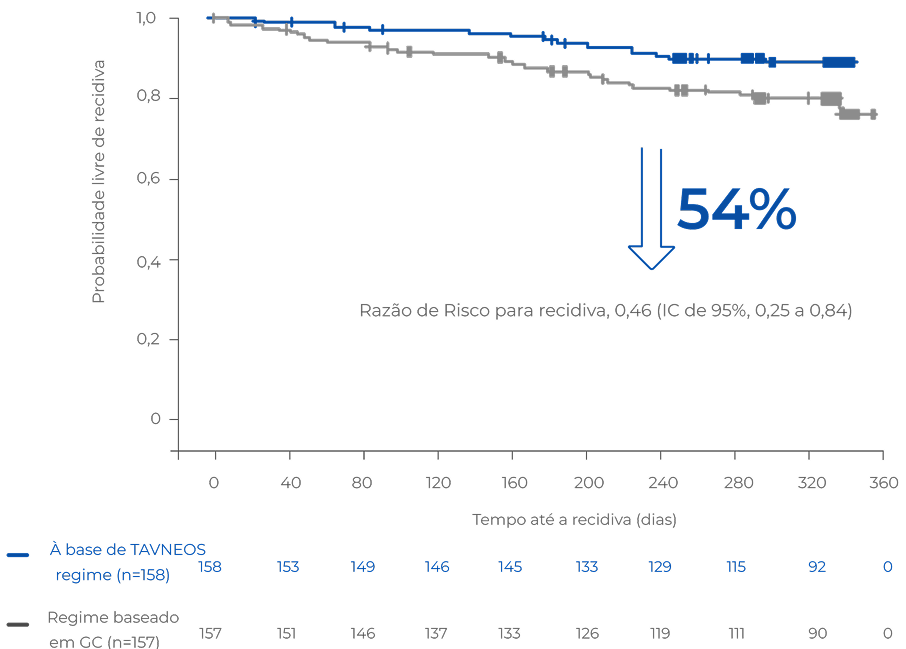
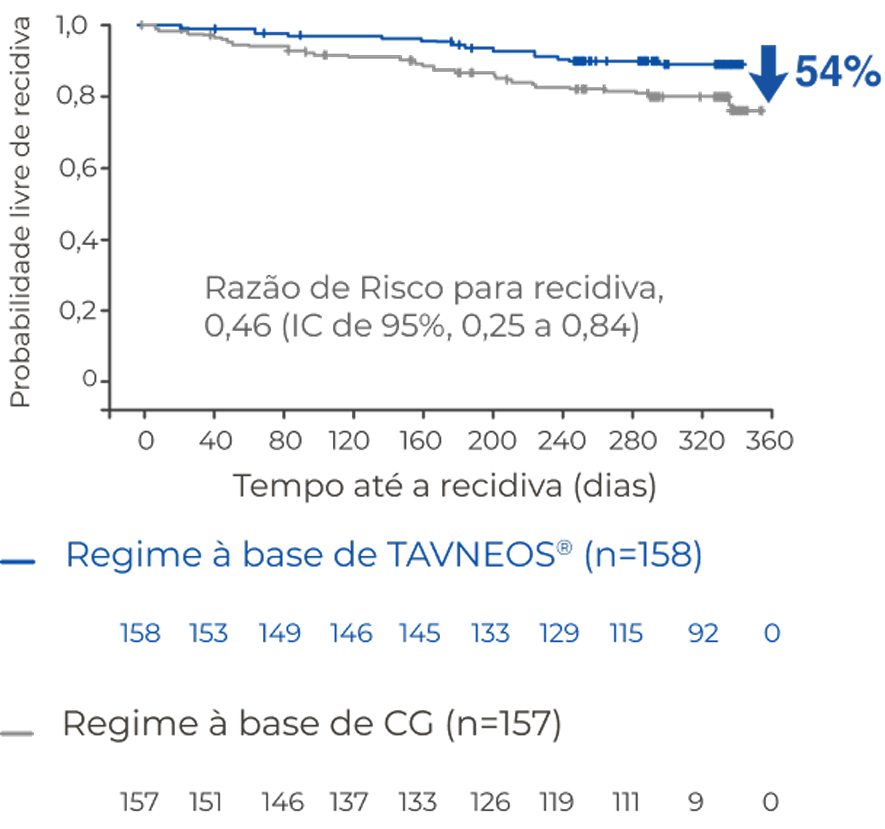
O regime baseado em TAVNEOS resultou em um menor risco absoluto de recidiva versus um regime baseado em GC ao longo de 52 semanas2
Risco absoluto de recidiva ao longo de 52 semanas de tratamento2
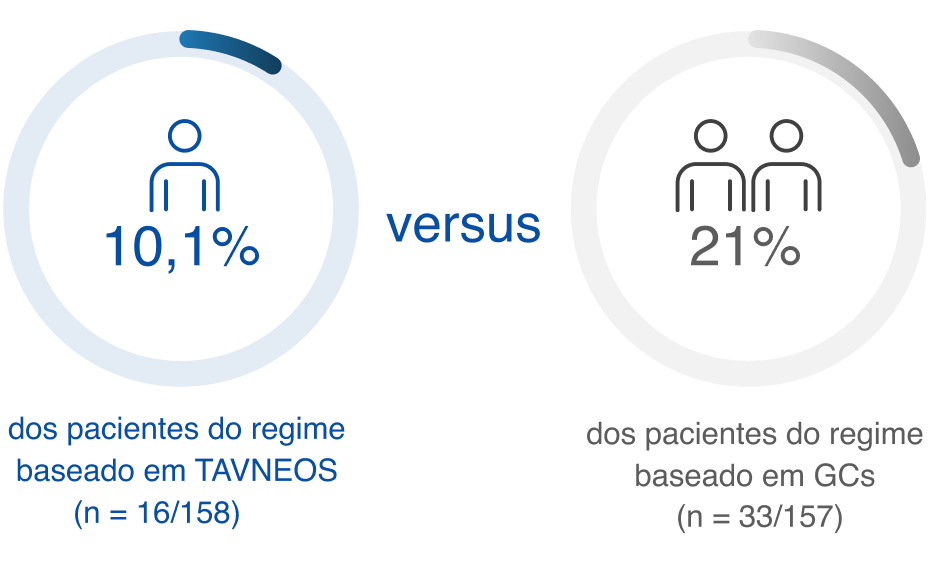

Os pacientes do grupo de GCs apresentaram duas vezes mais recidiva que o do grupo TAVNEOS2
Não houve um plano pré-especificado para ajuste dos intervalos de confiança para multiplicidade dos desfechos secundários; apenas estimativas pontuais e intervalos de confiança de 95% são apresentados, e nenhuma conclusão definitiva pode ser tirada a partir desses dados2
DESENHO DO ESTUDO ADVOCATE

Estudo pivotal fase 3, multicêntrico, internacional, comparador ativo, randomizado, duplo-cego, duplo-pareado, controlado, de 52 semanas, com pacientes randomizados para receber TAVNEOS 30 mg duas vezes ao dia (N=166) ou esquema de redução gradual de prednisona por 20 semanas (60 mg por dia reduzidos até a descontinuação na semana 21) (N=164) em adição à ciclofosfamida (seguido de azatioprina) ou ao rituximabe.2
Pacientes randomizados para o grupo TAVNEOS NÃO receberam GCs fornecidos pelo estudo. Os pacientes em ambos os regimes poderiam usar GCs não fornecidos pelo estudo durante todo o estudo de 52 semanas, a critério médico, por agravamento da VAA ou por outras razões clínicas. GCs fornecidos fora do estudo durante a triagem tiveram que ser reduzidos gradualmente para ≤20 mg por dia antes da entrada no estudo e posteriormente para 0 mg até o final da semana 4 do estudo.5
Principais critérios de inclusão e exclusão5
Critérios de inclusão
- ≥12 anos de idade*
- GPA ou PAM recém-diagnosticado ou em recidiva de acordo com as definições da Conferência de Consenso de Chapel Hill
- Indicado para tratamento com RTX ou CYC
- MPO+ ou PR3+
- TFGe estimada de ≥15 ml/min/1,73 m2
- Presença de pelo menos um item grave ou três não graves, ou pelo menos dois critérios renais de hematúria e proteinúria conforme a BVAS
Critérios de exclusão
- Hemorragia alveolar exigindo ventilação pulmonar invasiva com duração prevista para além da triagem
- Qualquer outra doença autoimune multissistêmica
- Coagulopatia ou distúrbio hemorrágico
- Exigiu diálise ou plasmaférese nas 12 semanas anteriores à triagem
- Transplante renal
- Ter recebido CYC em até 12 semanas antes da triagem, RTX em até 12 meses antes da triagem (ou até 6 meses caso haja reconstituição das células B, com contagem de CD19 >0,01x109/l), dose cumulativa de GCs IV >3 g em até 4 semanas ou GCs orais de >10 mg por dia de prednisona (ou equivalente) por >6 semanas continuamente antes da triagem
*Pacientes adultos e adolescentes com GPA/PAM participaram deste estudo. Para obter detalhes adicionais, acesse clinicaltrials.gov, código do estudo: NCT02994927
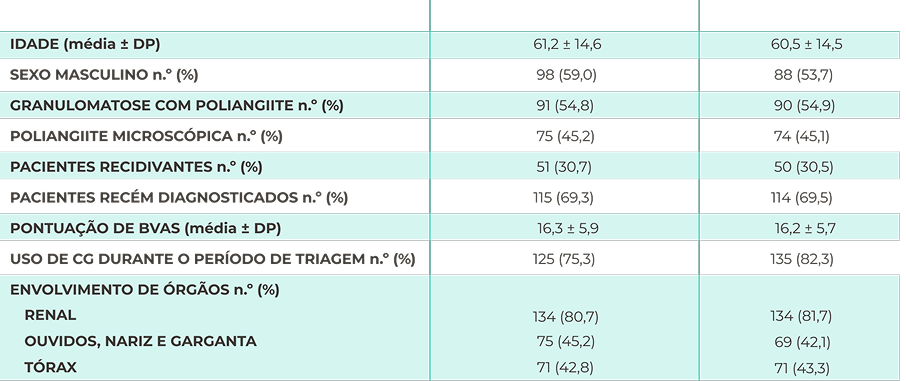
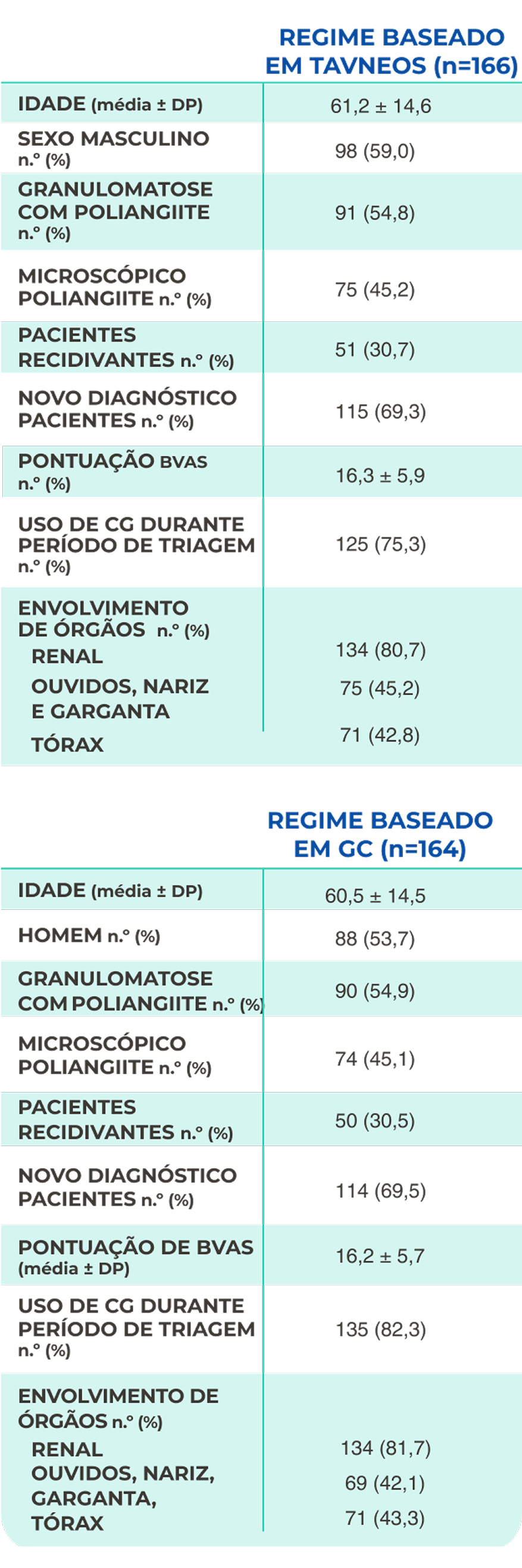
Características da avaliação inicial22
Desfechos primários2
Desfechos secundários2,5,6
Não houve um plano pré-especificado para ajuste dos intervalos de confiança em razão da multiplicidade dos desfechos secundários; apenas estimativas pontuais e intervalos de confiança de 95% são apresentados, e nenhuma conclusão definitiva pode ser tirada a partir desses dados2
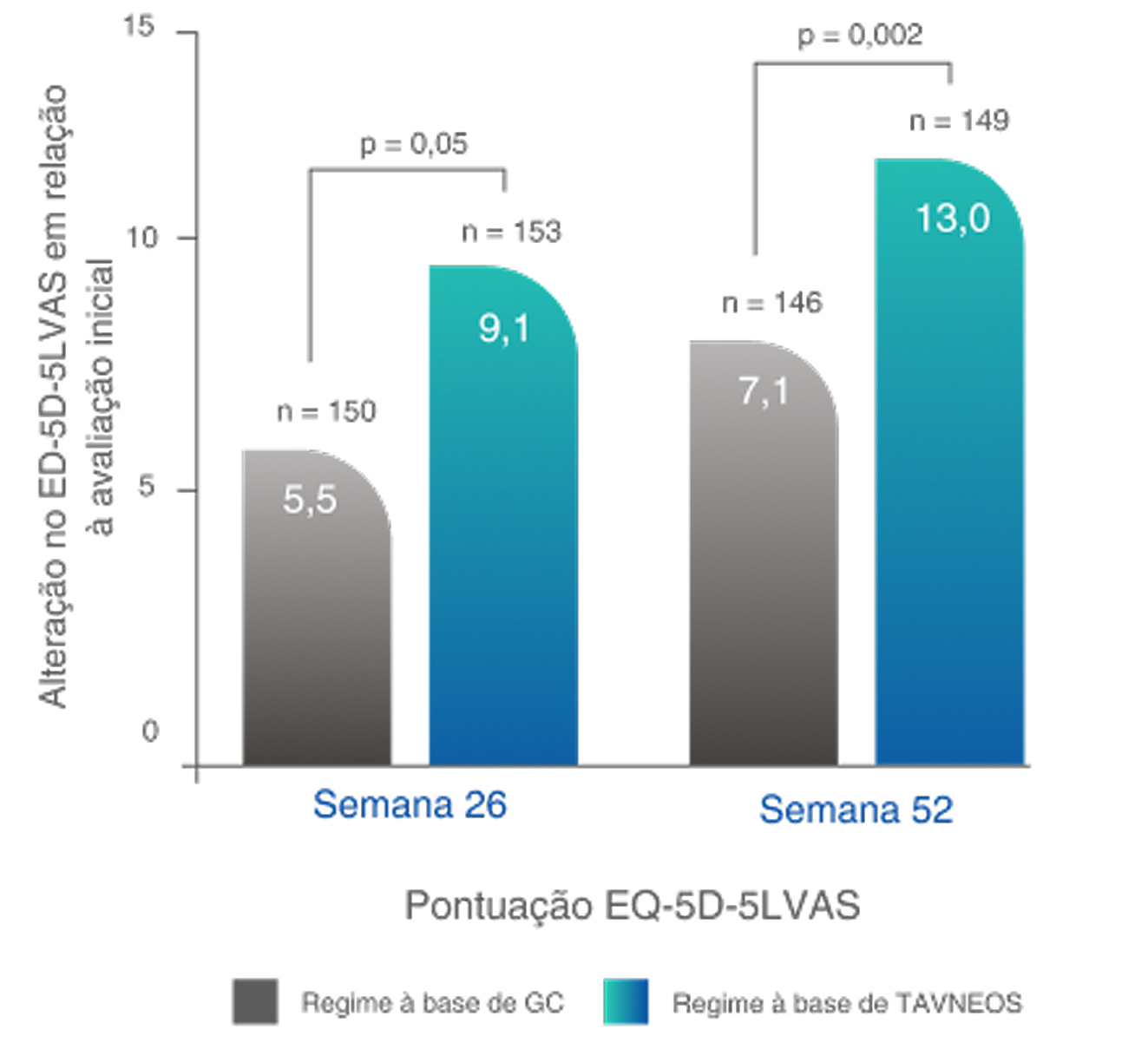
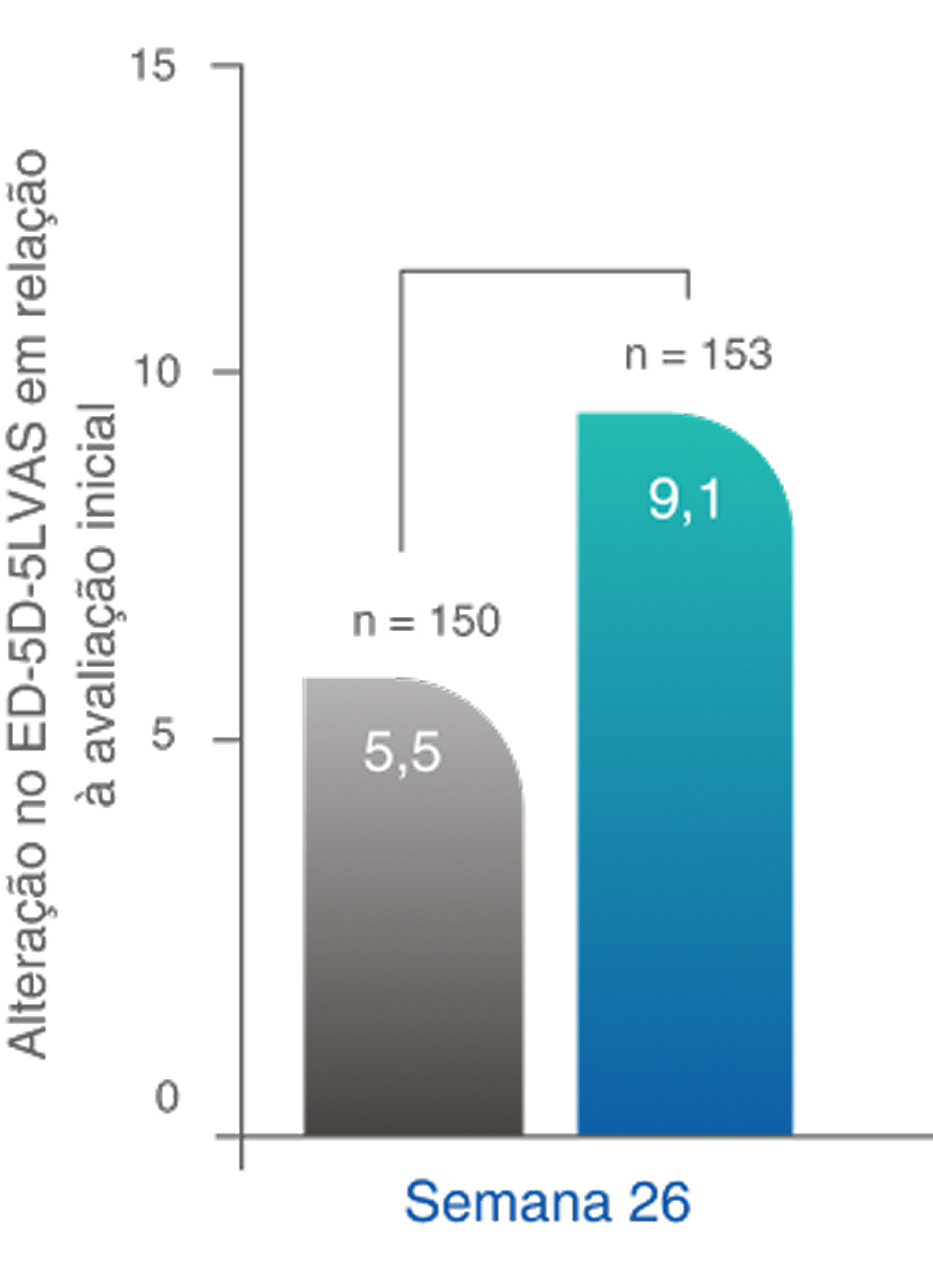
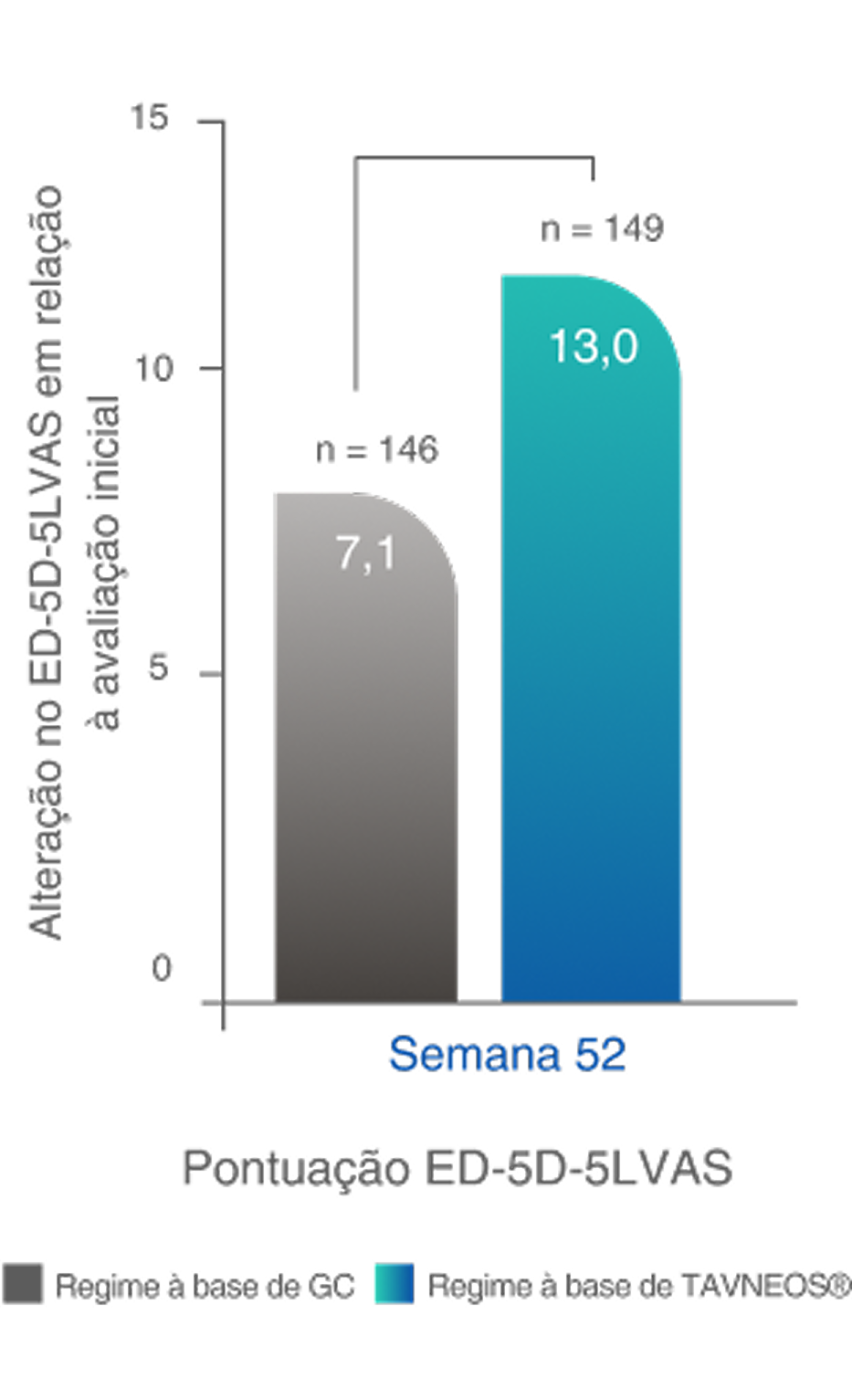
*A QoL relacionada à saúde foi medida usando duas pontuações: pontuação da EVA do EQ-5D-5L e índice do EQ-5D-5L. Foram observadas melhoras significativas na pontuação da EVA do EQ-5D-5L no regime baseado em TAVNEOS na semana 26 (p=0,05) e na semana 52 (p=0,002) comparado ao regime baseado em GC. Com o índice EQ-5D-5L, melhoras numéricas foram observadas na semana 26 e melhoras significativas foram observadas na semana 52 (p=0,009) no grupo TAVNEOS versus grupo de GC5,6
Desfecho secundário
MELHORA SUSTENTADA NA FUNÇÃO RENAL AO LONGO DE 52 SEMANAS

O grupo que recebeu TAVNEOS demonstrou melhoras significativas na TFGe2
Melhoras na TFGe em 26 e 52 semanas (desfecho secundário)2,7
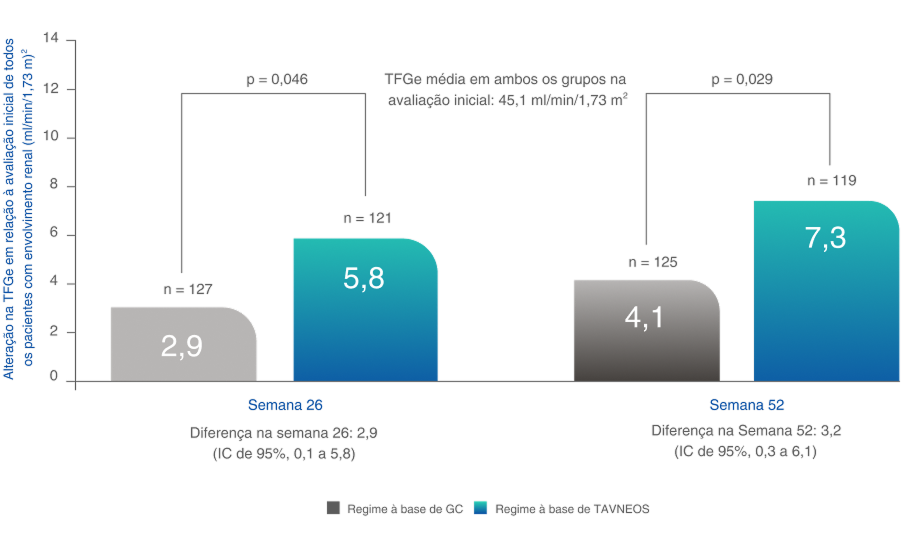
Análise post-hoc
Beneficios significativos especialmente em pacientes com a menor função renal na avaliação inicial2,7-9
Em pacientes com DRC em estágio 4 (TFGe <30 ml/min/1,73 m2):2,7-9

ml/min/1,73 m2 de aumento da TFGe no grupo TAVNEOS (n=52) versus +8,2 ml/min/1,73 m2 no grupo GC (n=48) na semana 52 (p=0,005) (diferença 5,6, IC de 95%, 1,7 a 9,5)
Em pacientes com DRC em estágio 4 (TFGe ≤ 20 ml/min/1,73 m2):7

mL/min/1,73 m2 de aumento da TFGe grupo TAVNEOS (n=27) versus +7,7 mL/min/1,73 m2 no regime baseado em GC (n=23) na Semana 52 (p=0,003) (diferença 8,4, IC de 95%, 2,9 a 13,8)
Não houve um plano pré-especificado para ajuste dos intervalos de confiança em razão da multiplicidade dos desfechos secundários; apenas estimativas pontuais e intervalos de confiança de 95% são apresentados, e nenhuma conclusão definitiva pode ser tirada a partir desses dados2
Desfecho secundário
TOXICIDADE DE GLICOCORTICOIDE REDUZIDA

Regime baseado em TAVNEOS demonstrou uma redução significativa na toxicidade de GC2,11

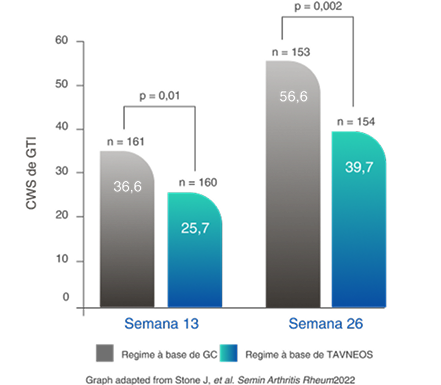
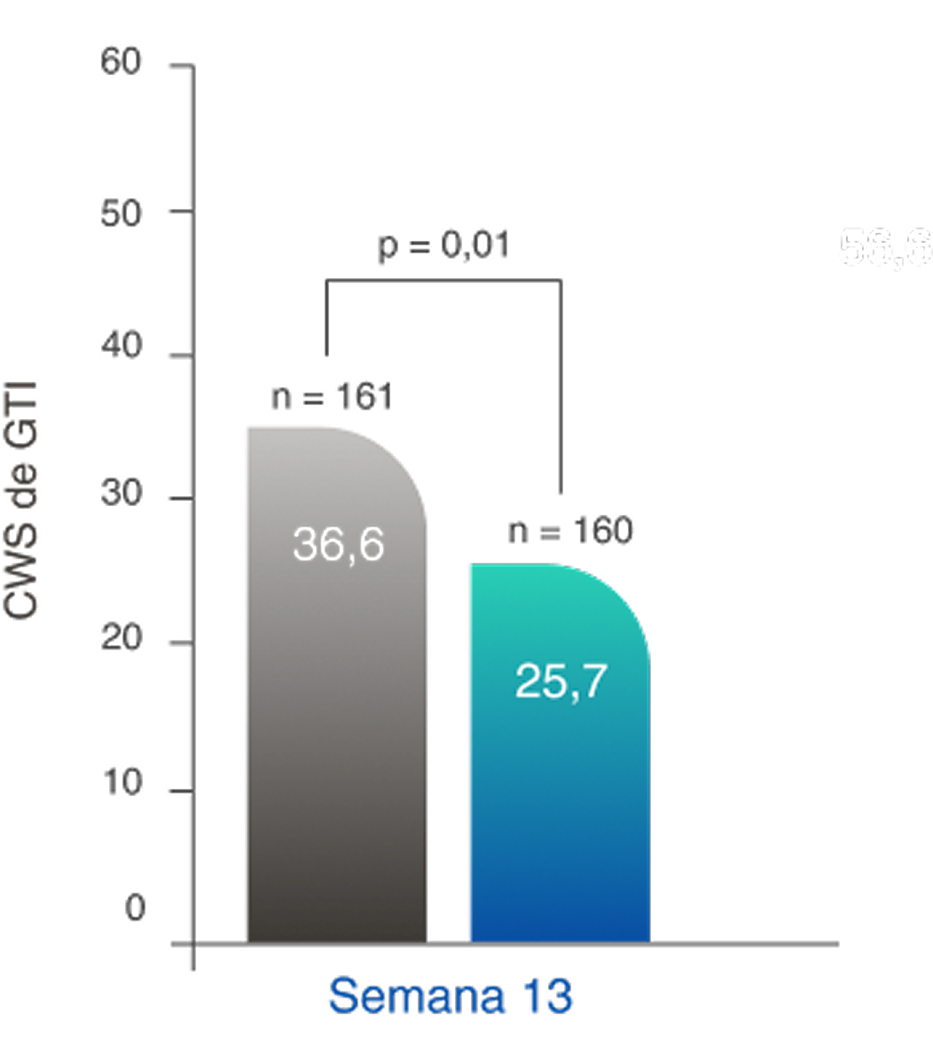
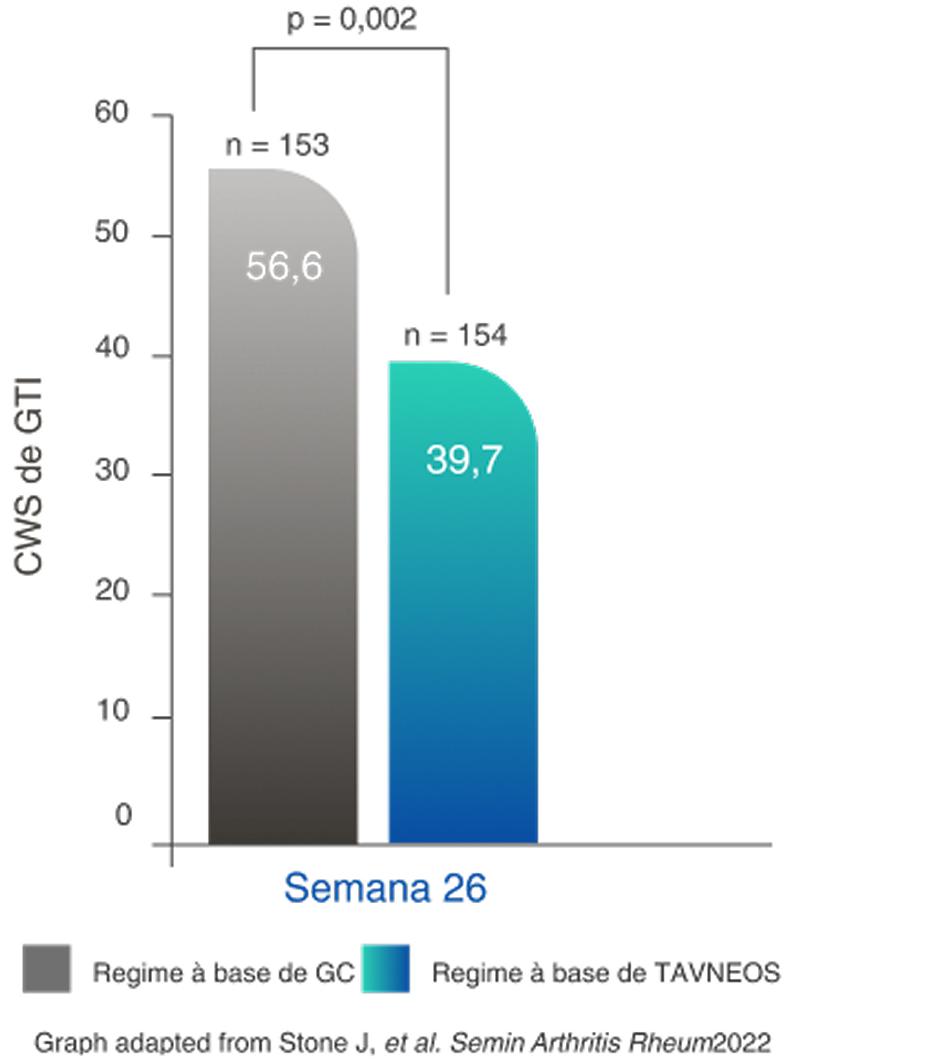
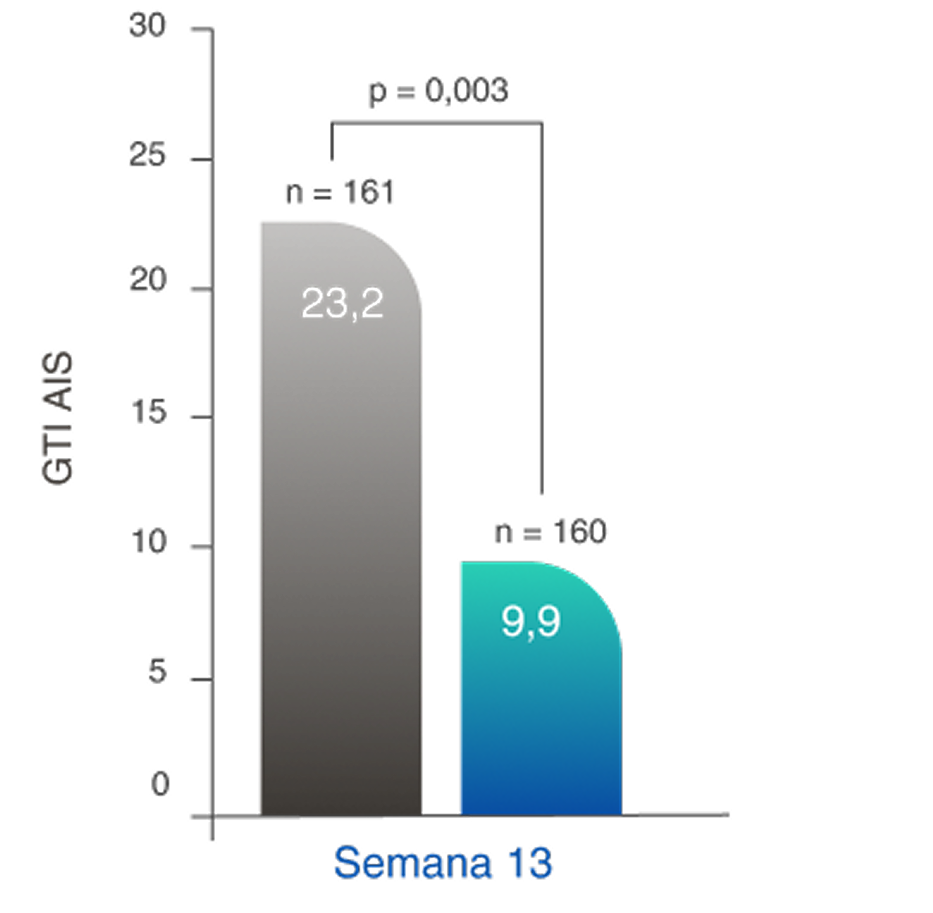
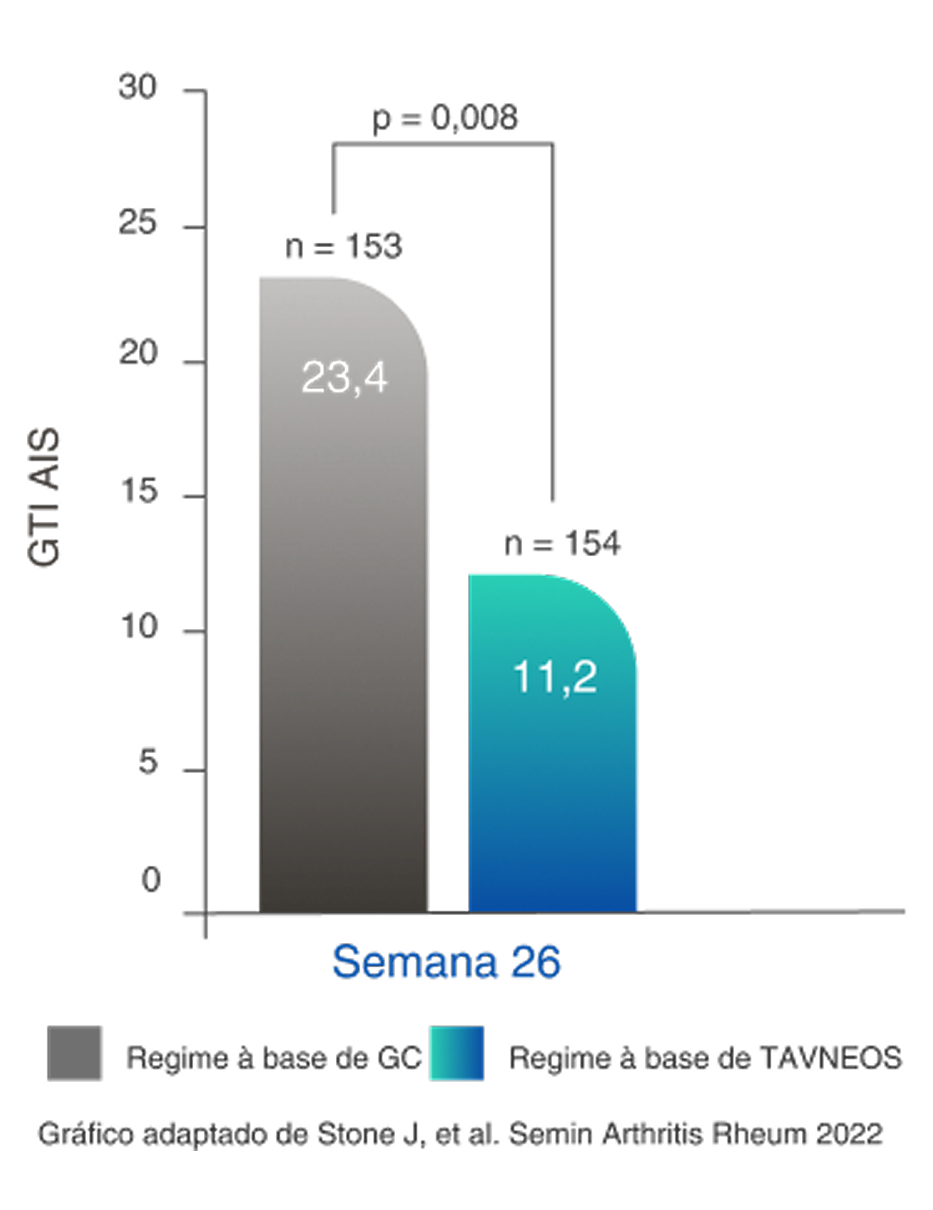
Redução na pontuação de agravamento cumulativa de GTI (PAC) no regime baseado em TAVNEOS versus regime baseado em GC na semana 262,11
Diferença na semana 13: -11,0 (IC de 95%, -19,7 a -2,2)
Diferença na semana 26: -16,8 (IC de 95%, -25,6 a -8,0)
Aumento da PAC da GTI conforme novas toxicidades são relatadas (p. ex., agravamento da hipertensão, infecção), mas não diminuem quando ocorrem melhoras12

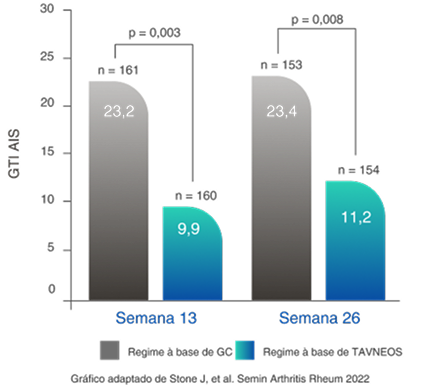
Redução na pontuação de melhora agregada de GTI (PMA) no regime baseado em TAVNEOS versus regime baseado em GC na semana 262,11
Diferença na semana 13: -13,3 (IC de 95%, -22,2 a -4,4)
Diferença na semana 26: -12,1 (IC de 95%, -21,1 a -3,2)
Aumento da PMA do GTI quando toxicidades são relatadas e diminuição quando ocorre melhora12
Não houve um plano pré-especificado para ajuste dos intervalos de confiança para multiplicidade dos desfechos secundários; apenas estimativas de pontos e intervalos de confiança de 95% são apresentados, e nenhuma conclusão definitiva pode ser tirada a partir desses dados2
Desfecho secundário
MELHOR QUALIDADE DE VIDA

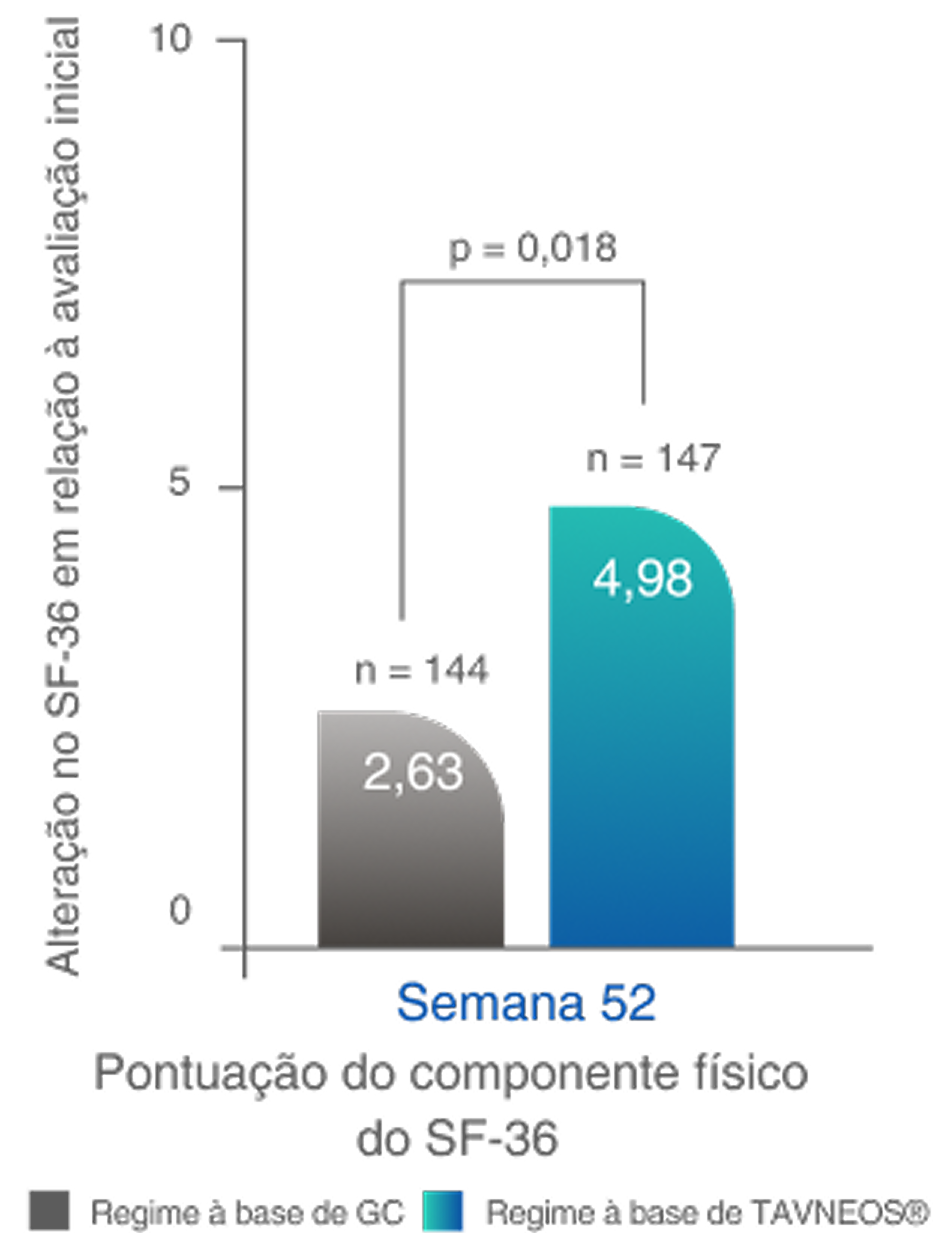
O regime baseado em TAVNEOS demonstrou melhoras significativas nos domínios físicos e relacionados à saúde da QoL2,10
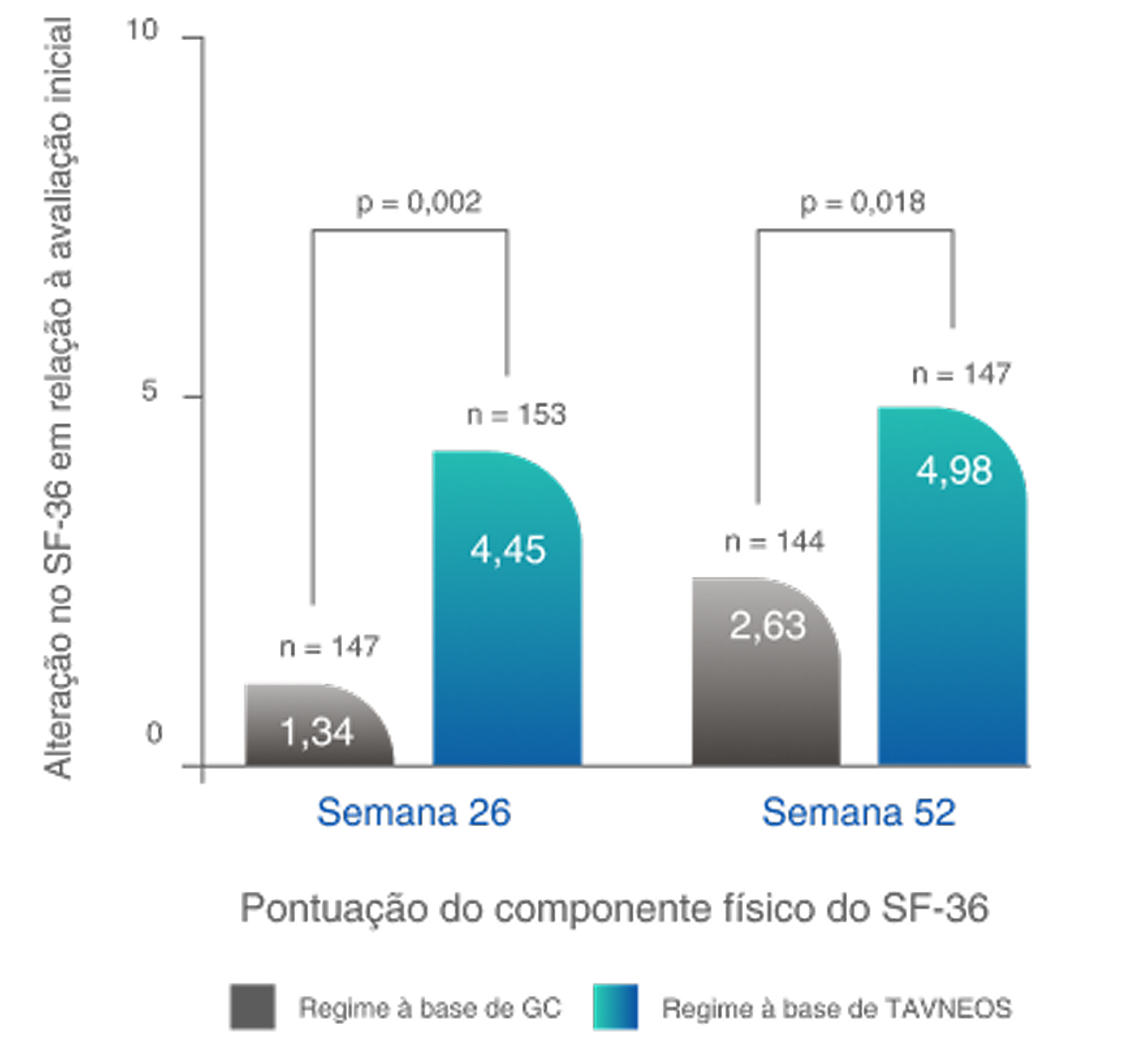
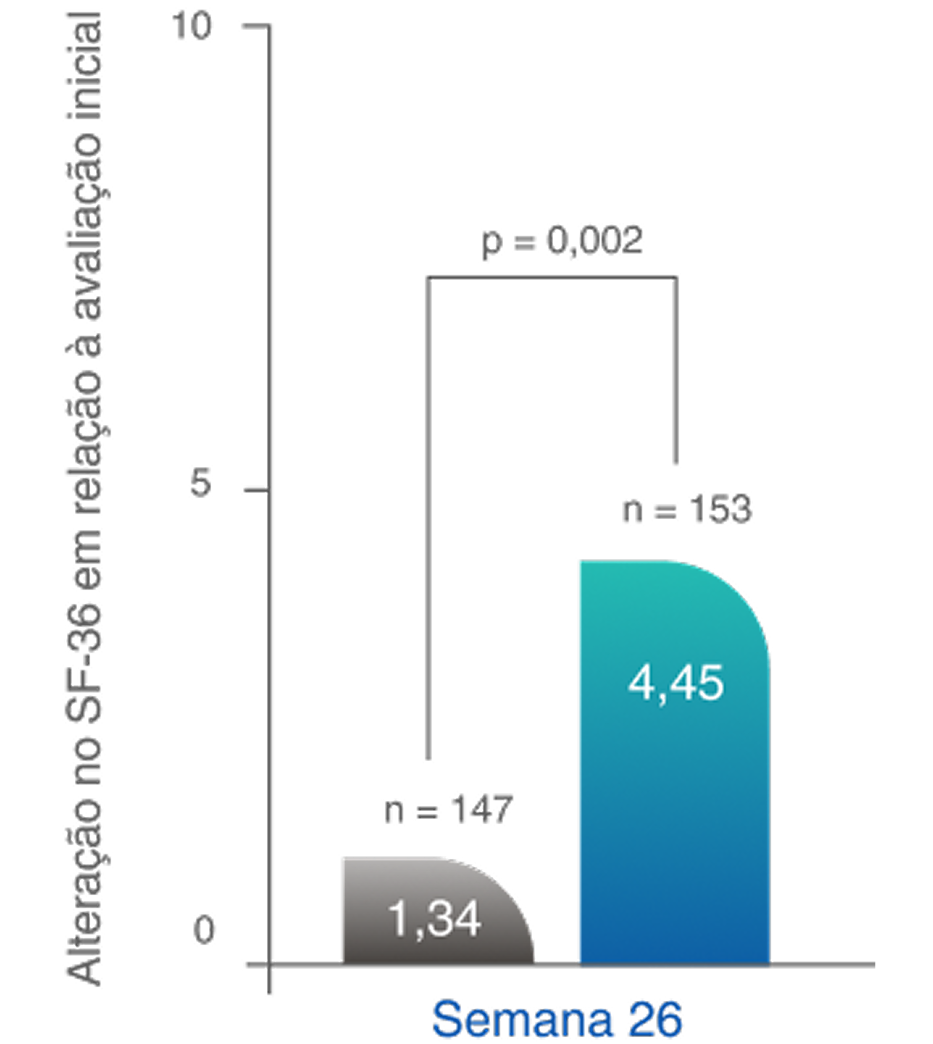
Melhoras significativas na QoL física na Semana 522,10‡
Diferença na semana 26: 3,10 (IC de 95%, 1,17 a 5,03)
Diferença na Semana 52: 2,35 (IC de 95%, 0,40 a 4,31)
Melhoras significativas na QoL relacionada à saúde na semana 521,10§
Diferença na semana 26: 3,6 (IC de 95%, -0,1 a 7,2)
Diferença na Semana 52: 5,9 (IC de 95%, 2,3 a 9,6)

ADVOCATE é o primeiro estudo a mostrar uma diferença significativa na QoL entre os grupos de tratamento2,5,13–15
Não houve um plano pré-especificado para ajuste dos intervalos de confiança para multiplicidade dos desfechos secundários; apenas estimativas de pontos e intervalos de confiança de 95% são apresentados, e nenhuma conclusão definitiva pode ser tirada a partir desses dados2
Referências e notas de rodapé
Notas de rodapé
*A remissão clínica no estudo ADVOCATE foi definida como BVAS 0 e nenhum uso de GC nas 4 semanas anteriores.2
†O NNT foi calculado usando https://www.statology.org/confidence-interval-difference-in-proportions-calculator/ para determinar os intervalos de confiança para a diferença bruta em proporções. Na semana 52, as taxas de resposta foram de 65,7% no grupo TAVNEOS e 54,9% no grupo de GC. Isso resultou em um resultado bruto de NNT = 1/(0,657-0,549) = 9,26, arredondado para 10 pacientes. Usando o modelo ajustado e a diferença comum estimada, o NNT = 1/0,125 = 8. Concluindo, o NNT fica entre 8 e 10 pacientes na semana 52.2
‡Foi observada uma melhora numérica na QoL mental.10
§Com o índice EQ-5D-5L, foram observadas melhoras numéricas na Semana 26 e melhoras significativas na Semana 52 (p=0,009) no grupo TAVNEOS versus regime baseado em GC.10
Abreviações
Abreviações
VAA, Vasculite associada ao ANCA; PMA, Pontuação de melhora agregada; ANCA, anticorpo anti-citoplasma de neutrófilos; PAVB, Pontuação da atividade da vasculite de Birmingham; CD19, grupo de diferenciação 19; IC, intervalo de confiança; DRC, doença renal crônica; PAC, Pontuação de agravamento cumulativa; CYC, ciclofosfamida; TFGe, taxa de filtração glomerular estimada; EQ-5D-5L, EuroQol 5 dimensões 5 níveis; GC, glicocorticoide; GPA, granulomatose com poliangeíte; GTI, Índice de toxicidade de glicocorticoides; IV, intravenoso; MCP-1, proteína quimiotática de monócitos-1; MOA, mecanismo de ação; PAM, poliangeíte microscópica; MPO, mieloperoxidase; NNT, número-necessário-para-tratar; PR-3 proteinase-3; QoL, qualidade de vida; RTX rituximabe; DP, desvio padrão; SF-36, Pesquisa de Saúde de Formulário Curto de 36 Itens ; UACR, razão albumina:creatinina urinária; EVA, escala visual analógica.
Referências
- TAVNEOS EU SmPC janeiro de 2025.
- Jayne D, et al. N Eng J Med 2021; 384(7): 599–609.
- Bekker P, et al. PLoS One 2016;11(10):e0164646.
- European Medicine Agency (2021). First-in-class medicine recommended for treatment of rare blood vessel inflammation. Available at: https://www.ema.europa.eu/en/news/first-class-medicine-recommended-treatment-rare-blood-vessel-inflammation. Date accessed: January 2025.
- Jayne D, et al. N Engl J Med 2021;384(7):599–609. [Supp Appendix].
- TAVNEOS EPAR. Available at: https://www.ema.europa.eu/en/documents/assessment-report/tavneos-epar-public-assessment-report_en.pdf. Data de acesso: janeiro de 2025.
- Cortazar F, et al. Kidney Int Rep 2023;8(4):860–70.
- Jayne D, et al. J Am Soc Nephrol 2021:32.
- NHS (2019). Chronic Kidney Disease. Available at: https://www.nhs.uk/conditions/kidney-disease/diagnosis/. Date accessed: January 2025.
- Strand V, et al. Lancet Rheumatol 2023;5:e451–60.
- Stone J, et al. Semin Arthritis Rheum 2022;55:152010.
- McDowell P, et al. J Allergy Clin Immunol Pract 2021;9(1):365–72.
- Stone JH, et al. N Engl J Med 2010;363(3):221–32.
- Walsh M, et al. N Engl J Med 2020;382(7):622–31.
- Charles P, et al. Ann Intern Med 2020;173(3):179–87.
▼ Este produto medicinal está sujeito a monitoramento adicional. Isso permitirá a rápida identificação de novas informações de segurança. Os profissionais de saúde são solicitados a relatar quaisquer suspeitas de reações adversas.
BR-AVA-2500003 | Data de preparação: julho de 2025